
本网讯(基础医学院)近日,我校基础医学院刘琼教授、黄孝天教授团队在疫苗佐剂研发方面取得重要进展,相关成果以“An engineered nano-vesicle adjuvant platform (ENAP) for cytokine delivery enables a novel antigen coordinated vaccine against Helicobacter pylori”为题发表在国际权威期刊Journal of Extracellular Vesicles上(国际细胞外囊泡学会ISEV会刊,IF=14.5)。该工作由南昌大学独立完成。
幽门螺杆菌感染是慢性胃炎、消化性溃疡及胃癌的主要病因。由于抗生素耐药性问题日益严重,疫苗接种成为有前景的防控策略。然而,传统佐剂主要诱导Th2型免疫应答,难以有效清除定植于胃黏膜的病原体;而强效佐剂如霍乱毒素存在安全隐患。因此,精准调控黏膜免疫应答成为该领域长期未解的瓶颈。
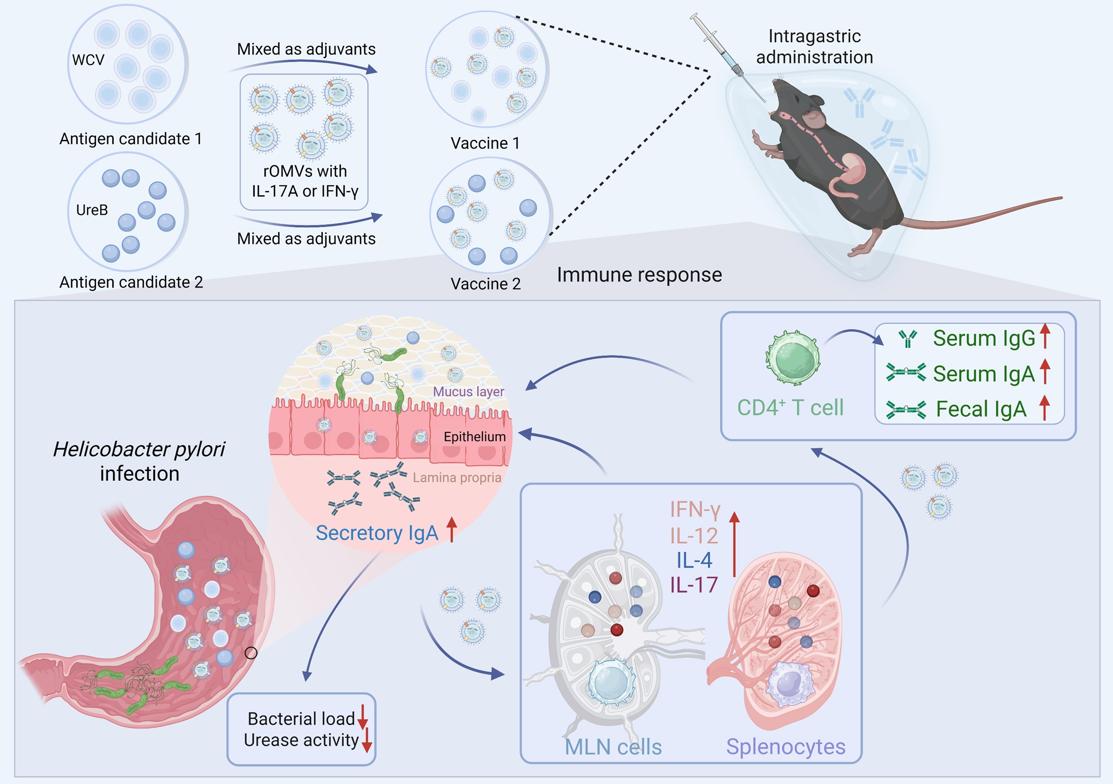
为此,研究团队构建了一种基于基因工程化幽门螺杆菌外膜囊泡的可编程细胞因子呈递平台(ENAP)。借助AI筛选,确定IL-17A和IFN-γ为最优细胞因子组合,首次验证了AI在佐剂设计中的可行性。团队还通过基因改造获得了低毒性的重组外膜囊泡(rOMVs),并利用电穿孔技术将编码上述细胞因子的质粒分别装载其中。小鼠模型显示,口服免疫后,该平台显著提升了抗原特异性血清IgG和胃黏膜sIgA水平,抗体应答持续12周以上,并诱导了平衡的Th1/Th2/Th17型细胞免疫应答。攻毒实验中,免疫组小鼠胃内幽门螺杆菌载菌量、脲酶活性和胃黏膜病理损伤均显著降低,双细胞因子联用效果优于单用,基因敲除模型进一步证实保护效应依赖于递送的细胞因子。该平台具有模块化、可编程特点,将传统佐剂发展为局部微环境重编程系统,为幽门螺杆菌疫苗研发提供了新工具,并具备良好的通用性,可快速适配其他黏膜病原体的疫苗开发需求。
该研究也是刘琼教授团队继2025年幽门螺杆菌重组外膜囊泡疫苗工作发表于Journal of Extracellular Vesicles上的又一项突破性成果,有效补充了幽门螺杆菌重组外膜囊泡疫苗在佐剂方面的不足,两项成果将有效推进基于外膜囊泡的高效病原疫苗转化落地。
基础医学院刘琼教授和黄孝天教授为本文的共同通讯作者,在读博士生尚银攀为第一作者。南昌大学为本文唯一通讯单位。该研究得到了国家自然科学基金、江西省自然科学基金和南昌大学基础医学院院内基金等课题资助。
论文链接:https://isevjournals.onlinelibrary.wiley.com/doi/10.1002/jev2.70274
审校:许航、涂金凤、朱文芳、陈小赤
